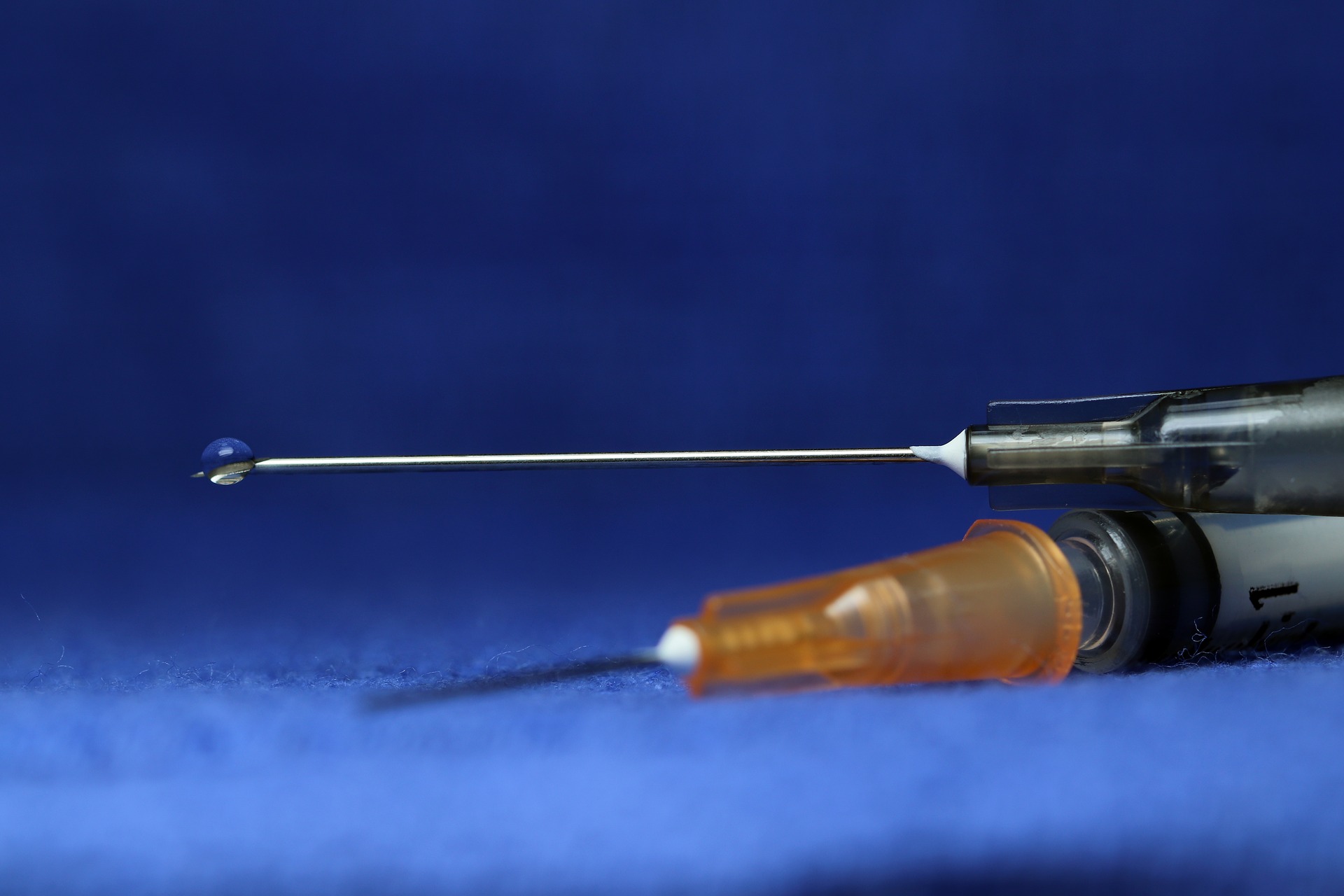
Studie ECZTRA 1 a 2 prokázaly účinnost tralokinumabu v terapii atopické dermatitidy
Monoklonální protilátka tralokinumab v klinických studiích fáze II výrazně zmírnila příznaky atopické dermatitidy v porovnání s placebem. Klinické studie fáze III nyní účinnost a bezpečnost monoterapie tralokinumabem potvrdily.
Úvod
Biologická léčba pronikla do oboru dermatitidy teprve před několika lety, ale zatím se jeví jako velmi slibná. Novým kandidátem na účinné biologikum pro léčbu atopické dermatitidy je tralokinumab. Jedná se o humánní monoklonální protilátku proti interleukinu 13 (IL-13), který hraje významnou roli v patogenezi atopické dermatitidy. Tralokinumab neutralizací IL-13 potlačuje zánět kůže. Ve studiích fáze II prokázal zmírnění projevů a příznaků u dospělých pacientů se středně těžkou až těžkou atopickou dermatitidou.
Design a metodika
Randomizované dvojitě zaslepené placebem kontrolované 52týdenní studie fáze III ECTRA 1 a 2 hodnotily účinnost a bezpečnost tralokinumabu (v dávce 300 mg subkutánně každé 2 týdny) u pacientů se středně těžkou až těžkou atopickou dermatitidou, kteří adekvátně nereagovali na topickou léčbu.
Primárním sledovaným parametrem bylo dosažení skóre 0 nebo 1 na škále IGA (Investigator’s Global Assessment) a alespoň 75% snížení skóre EASI (Eczema Area and Severity Index) v 16. týdnu léčby. Pacienti léčení tralokinumabem se skóre IGA 0 nebo 1 a/nebo EASI 75 v 16. týdnu byli znovu randomizováni k podávání tralokinumabu každé 2 týdny, každé 4 týdny nebo k podávání placeba po dobu 36 týdnů.
Výsledky
Ve studii ECZTRA 1 dosáhlo v 16. týdnu hodnoty skóre IGA 0/1 15,8 % pacientů ve skupině s tralokinumabem a 7,1 % pacientů ve skupině s placebem (rozdíl 8,6 %; 95% interval spolehlivosti [CI] 4,1–13,1; p = 0,002). Ve studii ECZTRA 2 činil podíl pacientů s IGA 0/1 v 16. týdnu 22,2 % ve skupině s tralokinumabem oproti 10,9 % ve skupině s placebem (rozdíl 11,1 %; 95% CI 5,8–16,4; p < 0,001).
Poklesu skóre EASI o ≥ 75 % ve studii ECZTRA 1 dosáhlo 25 % pacientů ve skupině s tralokinumabem a 12,7 % ve skupině s placebem (rozdíl 12,1 %; 95% CI 6,5–17,7; p < 0,001), ve studii ECZTRA 2 se jednalo o 33,2 % pacientů s tralokinumabem a 11,4 % s placebem (rozdíl 21,6 %; 95% CI 15,8–27,3; p < 0,001).
Nežádoucí účinky byly u pacientů s tralokinumabem hlášeny v 76,4 % ve studii ECZTRA 1 a v 61,5 % ve studii ECZTRA 2. Ve skupině s placebem se nežádoucí účinky objevily u 77,0 % pacientů ve studii ECZTRA 1 a u 66,0 % ve studii ECZTRA 2.
Závěr
Klinické studie ECZTRA 1 a 2 prokázaly superioritu monoterapie tralokinumabem v porovnání s placebem v terapii středně těžké až těžké atopické dermatitidy. Tralokinumab byl velmi dobře tolerován.
(svat)
Zdroj: Wollenberg A., Blauvelt A., Guttman-Yassky E., et al.; ECZTRA 1 and ECZTRA 2 study investigators. Tralokinumab for moderate-to-severe atopic dermatitis: results from two 52-week, randomized, double-blind, multicentre, placebo-controlled phase III trials (ECZTRA 1 and ECZTRA 2). Br J Dermatol. 2021 Mar; 184 (3): 437–449. Dostupné na https://pubmed.ncbi.nlm.nih.gov/33000465/.